Modelo atômico de Rutherford e Bohr
Este material é parte integrante do Jogo do Prêmio Nobel de Atomística
© Carlos Alberto dos Santos, Eliabe Maxsuel de Aquino, Farnésio Vieira Diniz
© Carlos Alberto dos Santos, Eliabe Maxsuel de Aquino, Farnésio Vieira Diniz
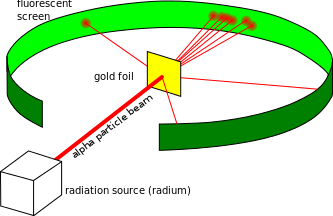
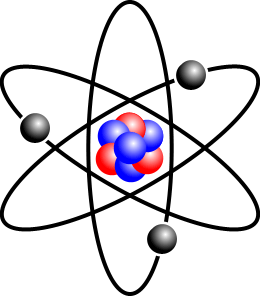
No texto sobre a história dos modelos atômicos, vimos que:
|
  |
Se é assim, podemos fazer algumas perguntas básicas:
- A que distância do núcleo esse elétron gira?
- Ele pode girar a qualquer distância do núcleo?
- Uma vez girando em determinada órbita, o elétron ficará para sempre nessa órbita?
- O que acontecerá se o elétron pular de uma órbita para outra?
Essas perguntas podem ser respondidas a partir do modelo de Bohr. Para isso você precisa ler os seguintes textos:
- Níveis de energia no átomo de Bohr.
- A constante de Planck e os níveis de energia no átomo de Bohr.
- Séries espectrais do átomo de hidrogênio.